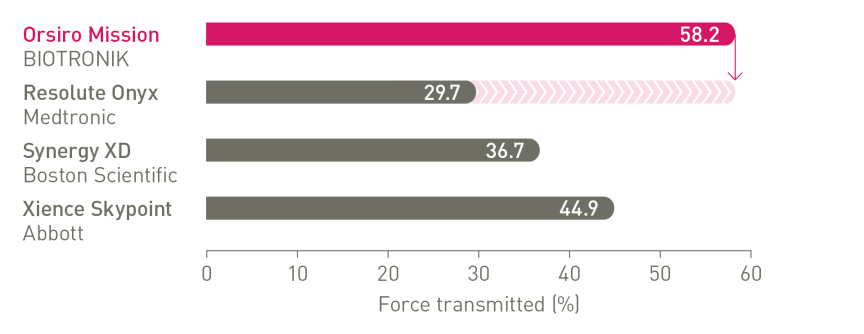
Líder en empuje⁴
Hasta un 96 % más de fuerza transmitida desde el conector a la punta
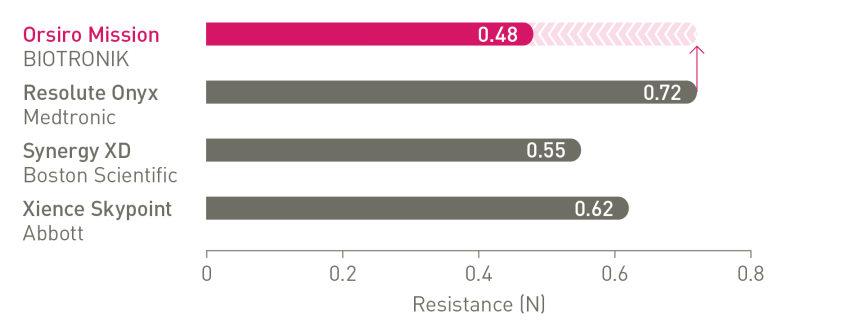
Líder en navegabilidad⁴
La fuerza necesaria para alcanzar la lesión se reduce hasta en un 33 %.
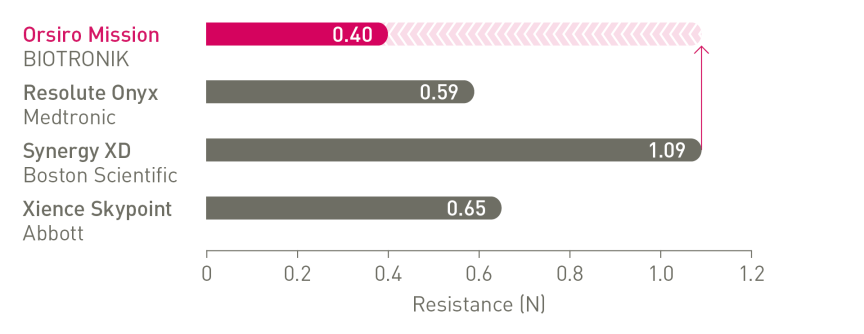
Líder en capacidad de cruce⁴
Hasta un 64 % menos de fuerza necesaria para cruzar con éxito anatomías complejas