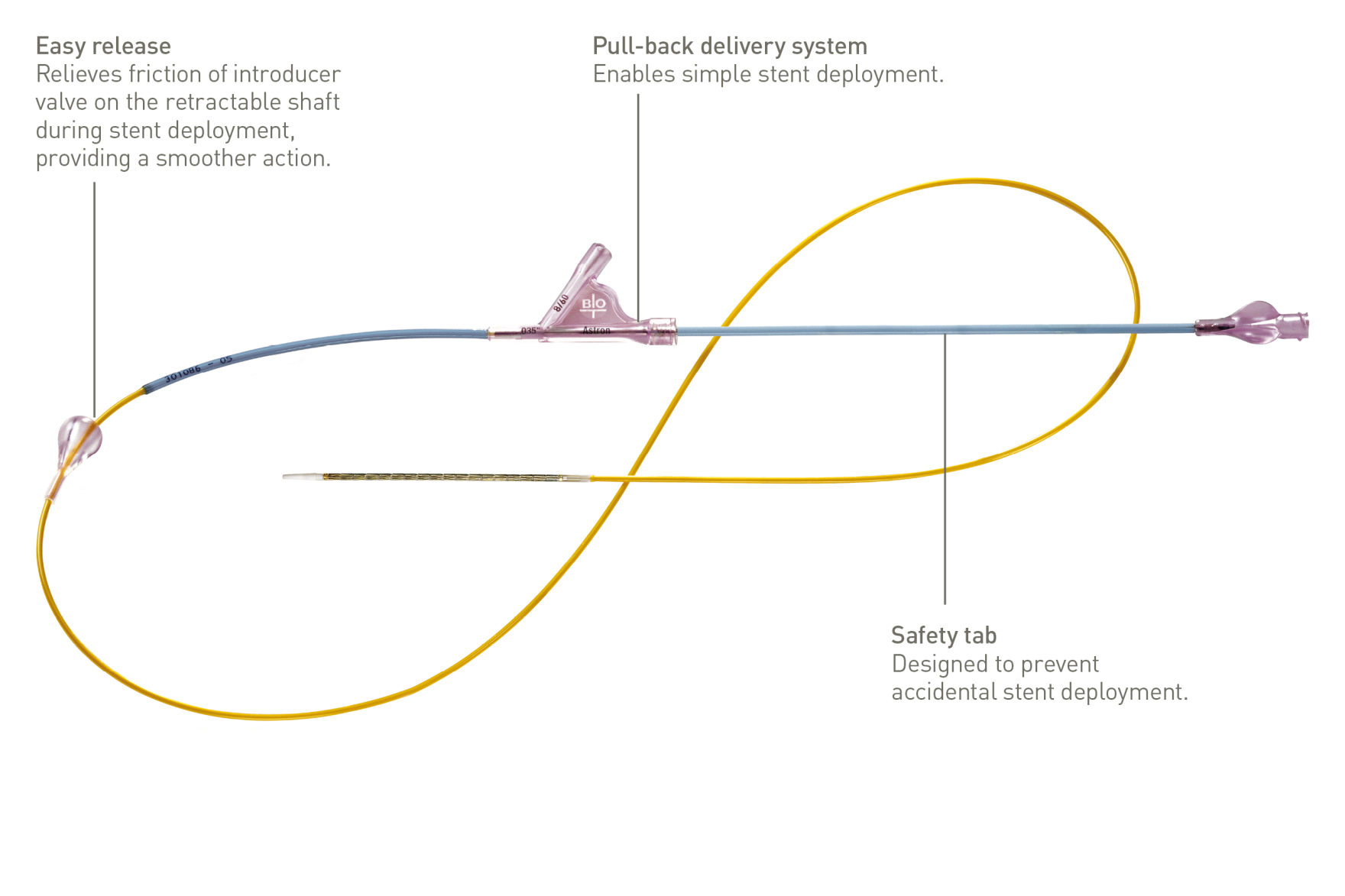
El diseño de stent segmentado y el grosor de strut se han concebido para lograr suficiente fuerza crónica expansiva en la región ilíaca, mientras que el diseño pico-valle y las conexiones articuladas en S proporcionan flexibilidad multidireccional y evitan la formación de escamas en arterias tortuosas.
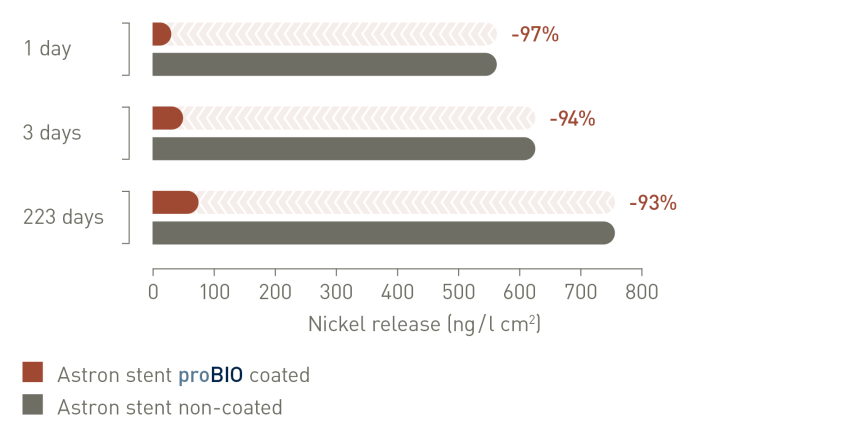
El revestimiento de carburo de silicioproBIO® reduce la liberación de iones al constituir una barrera eficaz y fiable frente a la liberación de iones de níquel y otros metales pesados.2