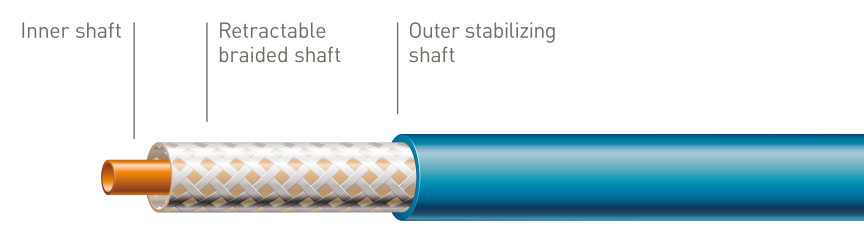
Einzigartiges triaxiales Schaftdesign
Der stabilisierende Außenschaft vermeidet Reibung zwischen dem zurückziehbarem Schaft und dem Ventil der Einführschleuse. Dies gewährleistet eine präzise Stentfreisetzung.
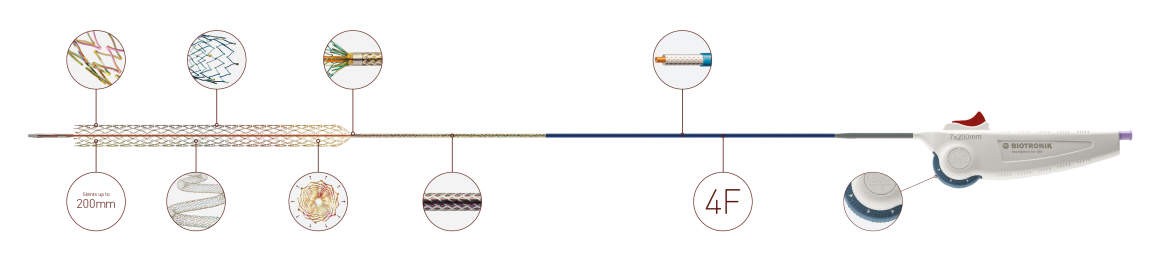
Pulsar-18 T3 ist der erste klinisch bewährte Stent mit dünnen Streben, der auf einem triaxialen Einführsystem mit geringem Profil (4 F) aufgebracht ist. Er ist indiziert für Patienten mit atherosklerotischen Erkrankungen der femoralen, proximalen poplitealen und infrapoplitealen Arterien und für die Behandlung bei unbefriedigenden Ergebnissen nach perkutaner transluminaler Angioplastie (PTA), wie z. B. Reststenose und Dissektion.*
Der stabilisierende Außenschaft vermeidet Reibung zwischen dem zurückziehbarem Schaft und dem Ventil der Einführschleuse. Dies gewährleistet eine präzise Stentfreisetzung.

| Stent | |
|---|---|
| Kathetertyp | OTW |
| Empfohlener Führungsdraht | 0,018” |
| Stentmaterial | Nitinol |
| Strebendicke | 140 μm |
| Strebenbreite | 85 μm |
| Stentbeschichtung | proBIO® (amorphes Siliziumkarbid) |
| Stentmarker | 6 Goldmarker an jedem Ende |
| Größen | Ø 4,0–7,0 mm; L: 20–200 mm |
| Schaft | 4 F, hydrophobe Beschichtung, triaxial |
| Arbeitslänge | 90 cm und 135 cm |
| Stent- ø (mm) |
Katheterlänge 90 cm |
||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 20** | 30 | 40 | 60 | 80 | 100 | 120 | 150 | 170 | 200 | ||
| 4 F | 4 | 430437 | 430438 | 430439 | 430440 | 430441 | 430442 | 430443 | 430444 | 430445 | 430446 |
| 5 | 430447 | 430448 | 430449 | 430450 | 430451 | 430452 | 430453 | 430454 | 430455 | 430456 | |
| 6 | 430457 | 430458 | 430459 | 430460 | 430461 | 430462 | 430463 | 430464 | 430465 | 430466 | |
| 7 | 430467 | 430468 | 430469 | 430470 | 430471 | 430472 | 430473 | 430474 | 430475 | 430476 | |
| **Nur auf Vorbestellung mit 8 Wochen Vorlauf | |||||||||||
| Stent- ø (mm) |
Katheterlänge 135 cm |
||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 20** | 30 | 40 | 60 | 80 | 100 | 120 | 150 | 170 | 200 | ||
| 4 F | 4 | 430477 | 430478 | 430479 | 430480 | 430481 | 430482 | 430483 | 430484 | 430485 | 430486 |
| 5 | 430487 | 430488 | 430489 | 430490 | 430491 | 430492 | 430493 | 430494 | 430495 | 430496 | |
| 6 | 430497 | 430498 | 430499 | 430500 | 430501 | 430502 | 430503 | 430504 | 430505 | 430506 | |
| 7 | 430507 | 430508 | 430509 | 430510 | 430511 | 430512 | 430513 | 430514 | 430515 | 430516 | |
| **Nur auf Vorbestellung mit 8 Wochen Vorlauf | |||||||||||
FTLR = Freiheit von Zielläsionsrevaskularisierung
1. BIOTRONIK Daten im Archiv. 2. Zhao HQ. Late stent expansion and neointimal proliferation of oversized nitinol stents in peripheral arteries. Cardiovasc Intervent Radiol. 2009 Jul;32(4):720-6. 3. Bosiers M. et al. 4-French – compatible endovascular material is safe & effective in the treatment of femoropopliteal occlusive disease: Results of the 4EVER Trial. ENDOVASC THER 2013. 20: 746-756. 4. Koskinas C. Role of endothelial shear stress in stent restenosis and thrombosis: pathophysiologic mechanisms and implications for clinical translation. JACC 2012 10; 59(15):1337-49. 5. Koppara T. Thrombogenicity and early vascular healing response in metallic biodegradable polymer-based and fully bioabsorbable drug-eluting stents. Circ Cardiovasc Interv. 2015 8(6):e002427
* Indikation gemäß Gebrauchsanweisung. Pulsar und proBIO sind Marken oder eingetragene Marken der Unternehmensgruppe BIOTRONIK.