BIOSOLVE-II
NCT01960504
Primer estudio con humanos de la 2.ª generación de andamios metálicos reabsorbibles farmacoactivos DREAMS
Conclusiones
- Magmaris demostró una seguridad y rendimiento favorables hasta el seguimiento de 24 meses.
- El índice de trombosis del andamio precisa o probable permaneció en el 0 % a los 24 meses.
Diseño del estudio
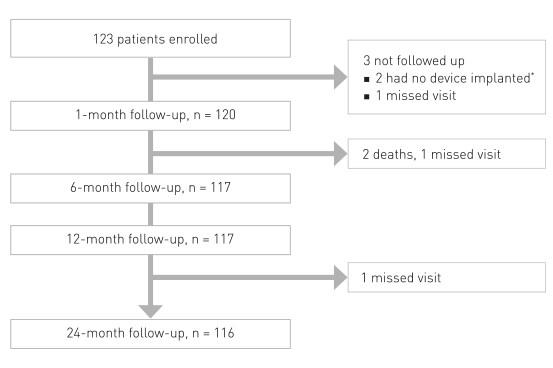
Ensayo prospectivo y multicéntrico (y el primero en humanos) para evaluar la seguridad y el rendimiento de Magmaris en 123 pacientes con un máximo de dos lesiones de novo en dos arterias coronarias independientes
Investigador principal:
Prof. Michael Haude (Neuss, Alemania)
* Se empleó a dos pacientes a los que no se sometió a implantes para calcular solo el éxito del dispositivo y los procedimientos.
Criterio de valoración principal:
Pérdida tardía de lumen (LLL) en segmento en el seguimiento de 6 meses
Criterios de valoración secundarios (seleccionados):
- TLF definido como una combinación de muerte súbita cardíaca, infarto de miocardio asociado al vaso tratado y revascularización de la lesión tratada controlada clínicamente (CD-TLR) a los 24 meses
- Trombosis del andamio precisa o probable a los 24 meses
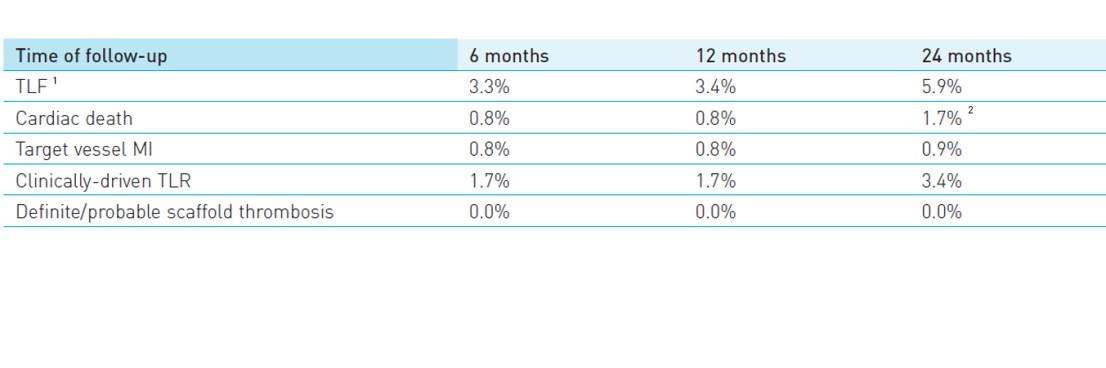
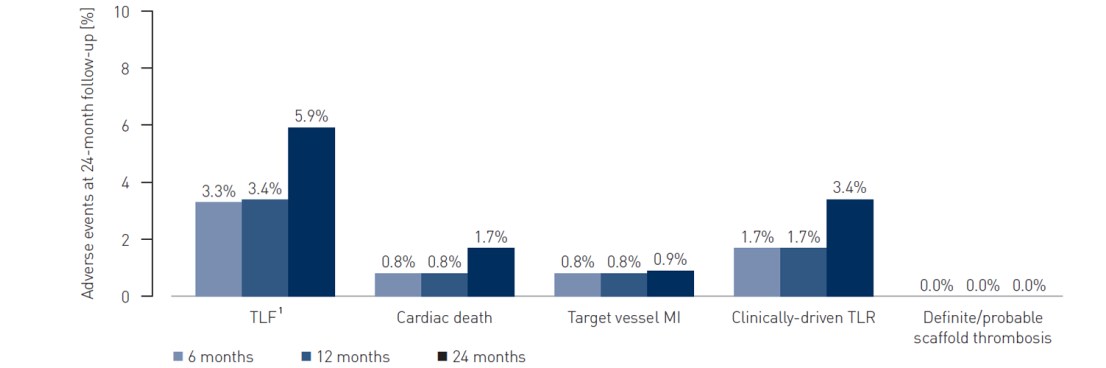
Resultados clínicos
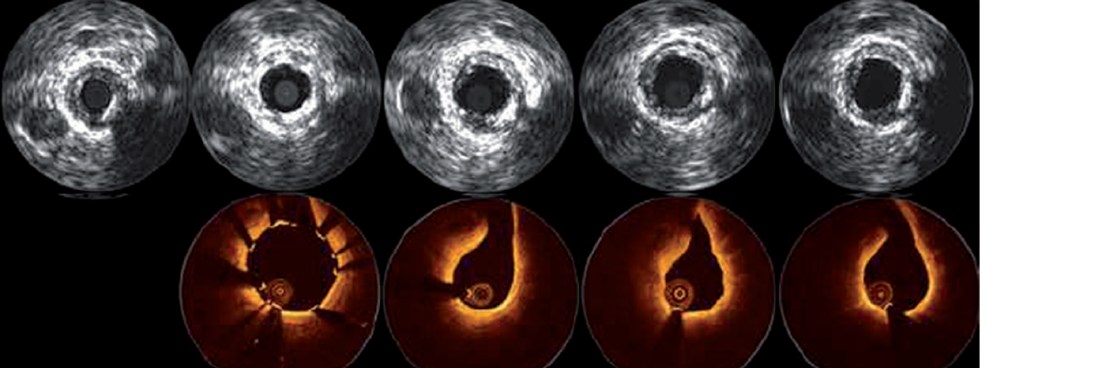
Descargas


Intervención vascular
Estudio clínicoPrimer ensayo en humanos con DREAMS (andamio metálico absorbible farmacoactivo)
Aviso legal
Magmaris no se encuentra disponible en EE. UU.
© BIOTRONIK AG – Todos los derechos reservados. Las especificaciones pueden modificarse, revisarse y mejorarse.
1 TLF definido como una combinación de muerte súbita cardíaca, IM asociado al vaso tratado y CD-TLR
2 Dos fallecimientos por causa desconocida adjudicadas como muertes súbitas cardíacas
